Простые Химические Домашние Опыты
 Химические опыты с порохом: как взрывается порох!
Химические опыты с порохом: как взрывается порох!
Дымный, или чёрный, порох представляет собой смесь калийной селитры (нитрата калия - KNO3), серы (S) и угля (C). Он воспламеняется при температуре около 300 °С. Порох может взрываться и от удара. В его состав входят окислитель (селитра) и восстановитель (уголь). Сера также является восстановителем, но главная её функция — связывать калий в прочное соединение. При горении пороха протекает реакция:
2KNO3+ЗС+S→ K2S+N2+3СО2,
- в результате которой выделяется большой объём газообразных веществ. С этим и связано использование пороха в военном деле: образующиеся при взрыве и расширяющиеся от тепла реакции газы выталкивают пулю из оружейного ствола. В образовании сульфида калия легко убедиться, понюхав ствол ружья. Он пахнет сероводородом — продуктом гидролиза сульфида калия.
 Химические опыты с селитрой: огненная надпись
Химические опыты с селитрой: огненная надпись
Эффектный химический опыт можно провести, имея калийную селитру. Напомню, что селитры - это сложные вещества - соли азотной кислоты. В данном случае нам понадобится калиевая селитра. Её химическая формула KNO3. На листе бумаги нарисуйте контур, рисунок (для большего эффекта пусть линии не пересекаются!). Приготовьте концентрированный раствор нитрата калия. Для сведений: в 15 мл горячей воды растворяется 20 г KNO3.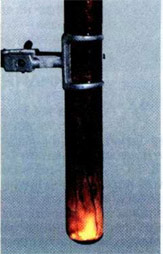 Затем с помощью кисти пропитываем бумагу по нарисованному контуру, при этом не оставляем пропусков и промежутков. дадим бумаге высохнуть. Теперь надо коснуться горящей лучинкой какой-нибудь точки на контуре. Тотчас же появится "искра", которая будет медленно двигаться по контуру рисунка, пока не замкнёт его полностью. Вот что происходит: Калиевая селитра разлагается по уравнению:
Затем с помощью кисти пропитываем бумагу по нарисованному контуру, при этом не оставляем пропусков и промежутков. дадим бумаге высохнуть. Теперь надо коснуться горящей лучинкой какой-нибудь точки на контуре. Тотчас же появится "искра", которая будет медленно двигаться по контуру рисунка, пока не замкнёт его полностью. Вот что происходит: Калиевая селитра разлагается по уравнению:
2KNO3→ 2 KNO2 +O2.
Здесь KNO2 +O2 - соль азотистой кислоты. От выделяющегося кислорода бумага обугливается и сгорает. Для большего эффекта опыт можно проводить в тёмном помещении.
Химические опыт растворения стекла в плавиковой кислоте
Стекло растворяетсяв плавиковой кислоте









